作者简介:吴田,博士,副教授通信作者:蓝增全,教授; E-mail:2351417655@qq.com
(1.西南林业大学园林学院,云南昆明 650224;2.西南林业大学环境科学与工程学院,云南昆明 650224;3. 北京林业大学生物科学与技术学院,北京 100083)
(1.College of Horticulture and Gardening, Southwest Forestry University, Kunming 650224, Yunnan, China; 2.College of Environment Science and Engineering, Southwest Forestry University, Kunming 650224, Yunnan, China; 3. College of Biological Science and Technology, Beijing Forestry University, Beijing 100083, China)
gene cloning; reference control gene; sequence analysis; expression analysis
DOI: 10.14067/j.cnki.1673-923x.2018.02.003
备注
作者简介:吴田,博士,副教授通信作者:蓝增全,教授; E-mail:2351417655@qq.com
为了解决诺丽实时荧光定量 PCR(qRT-PCR)检测中无内参基因的现状,根据其他植物 Actin基因的保守序列设计一对简并性引物,以诺丽果实总 RNA反转录成 cDNA为模板,进行 PCR扩增,扩增出的基因片段克隆到 pMD-18T载体,阳性克隆经 PCR鉴定后测序。序列结果表明:该片段长 393 bp,编码 131个氨基酸;所得序列与麦蓝菜 actin 1有最高的一致性( 96%)和相似性( 98%)。qRT-PCR结果表明,诺丽 Actin基因在诺丽的各个组织、果实不同发育时期都能稳定表达,且表达水平基本一致,适合在诺丽基因表达研究中作为内参基因。
In order to solve the problem of the lack of reference control gene in real-time fluorescence quantitative PCR (qRT-PCR) of noni, the degenerate primers were designed based on the conserved sequences of Actin genes from the other plants and the cDNA was reverse-transcribed from total RNA as template and amplified using PCR, and the gene fragment was cloned into pMD-18T vector. The positive clone was sequenced after being identified by PCR. The sequencing results revealed that the fragment of Actin gene from noni contained 393 bp, encoding a protein of 131 amino acids. Homology comparison with other plants actin sequences in GenBank showed that it shared the highest identities (96%) and positives (98%) with actin 1 of Vaccaria hispanica. The qRT-PCR indicated that the noni Actin gene was stable expression in various organs and in different fruit development periods,and the expression levels were basically consistent, so it was suitable as a reference control gene for the analysis of noni gene expression.
引言
植物肌动蛋白( Actin)是植物中普遍存在的重要蛋白质,参与了细胞分裂、细胞形成、胞内号传导、胞内物质运输、程序化死亡等重要生理功能 [1-5]。研究者已经在许多高等植物中克隆得到了 Actin基因,如茶树 [6]、向日葵 [7]、花生 [8]、碱蓬 [9]、木薯 [10]、芍药 [11]、海州香薷 [12]、山药 [13] 等。随着一系列高等植物 Actin基因的克隆,发现这些基因高度相似,氨基酸序列的同源性较高,一般在 70%以上 [14],具有组成型表达、易于扩增信等优点,因此可以作为重要的内参基因用于定量、半定量 PCR研究中,以比较不同来源的目的基因表达量的差异 [15]。诺丽 Morinda citrifolia Linn.属茜草科,在国外主要分布于美国的夏威夷、澳大利亚、印度尼西亚、印度的热带、亚热带等地区,在我国可以生长于西双版纳、海南及台湾南部等地区 [16]。诺丽被原产地的人们用作食材和药物已经有 2000多年的时间 [17],诺丽的叶可以止疼消炎 [18],果实的营养丰富,含有丰富的维生素 A、维生素 C、烟酸、钾、锰、硒以及其他有效成分 [19],具有较高的保健价值。近几年,国内外对诺丽的研究多专注于其药用成分、临床试验等,笔者没有检索到关于诺丽基因表达方面的研究,在一定程度上不利于诺丽应用机理的阐述。目前,在 GenBank中尚未有诺丽 Actin基因的报道,因此,获取诺丽 Actin基因,分析其表达特性,以确定其是否能够作为诺丽内参基因使用,对后续诺丽功能基因的研究具有重要意义。本研究拟根据其他植物 Actin基因的保守序列设计一对简并性引物,以诺丽果实总 RNA反转录成 cDNA后作为模板,进行诺丽 Actin基因克隆和序列比对分析,同时结合实时荧光定量 PCR(real-time fluorescence quantitative PCR,qRT-PCR)技术研究其在诺丽叶片、茎段、花以及不同发育时期的果实中的表达,旨在为诺丽内参基因的确定、诺丽生长发育中肌动蛋白的作用、其他基因在诺丽中的表达和调控奠定基础。
1 材料与方法
2 结果与分析
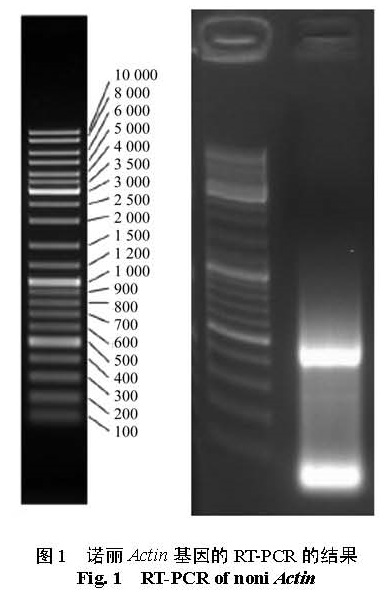
2.1 诺丽 Actin基因片段的克隆提取的总 RNA经凝胶电泳检测,发现其完整性好、纯度高,可以用于诺丽 Actin基因的克隆及 qRT-PCR分析。以总 RNA反转录所得到的第一链 cDNA为模板,P1、P2为引物进行 PCR 扩增。电泳检测发现,约在 400 bp 处有一条 PCR亮带,与预测片段大小一致(图1),推测是诺丽 Actin基因片段。将该目的片段回收纯化,经 PCR检测得到阳性克隆,片段大小约为 400 bp,可以进行测序。
2.2 诺丽 Actin基因的序列分析测序得到一段 393 bp的序列,编码 131个氨基酸。将该片段在 NCBI网站进行 Blastx比较,结果表明其与 actin 1(麦蓝菜, Vaccaria hispanica)有最高的一致性( identities)和相似性
(positives),分别为 96%和 98%,与 actin4(枇杷, Eriobotrya japonica)、actin 2(姜花, Hedychium coronarium)、actin(鹅掌楸, Liriodendron tulipifera)、actin(枸杞, Lycium chinense)等均有较高的一致性和相似性(图2),进一步表明克隆得到的是诺丽 Actin基因片段。
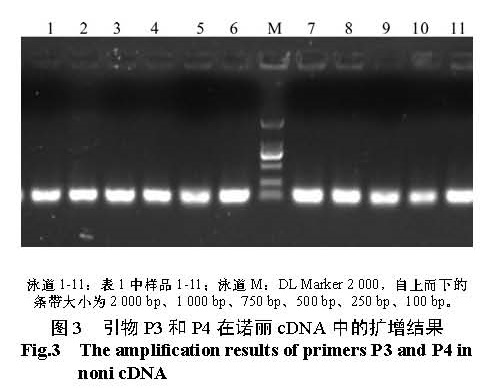
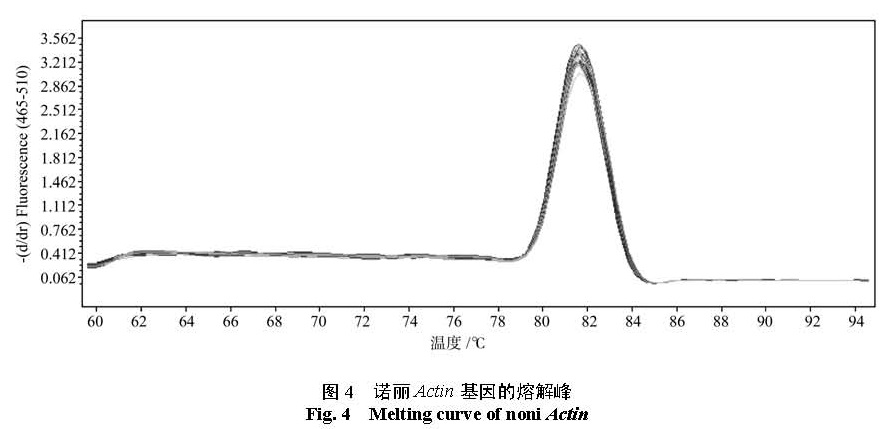
2.3 诺丽 Actin基因的定量分析利用 P3和 P4引物进行普通 PCR 扩增,琼脂糖凝胶电泳结果显示扩增产物长度为 111 bp,与预期长度一致,无引物二聚体和非特异条带(图3)。对荧光定量 RT-PCR产物进行熔解峰分析(图4),诺丽 Actin基因片段在 Tm=82 ℃处显示特异性单峰,进一步说明扩增产物无引物二聚体及非特异性扩增,同时也说明引物设计的合理性和特异性, PCR反应条件得到了较好的优化。
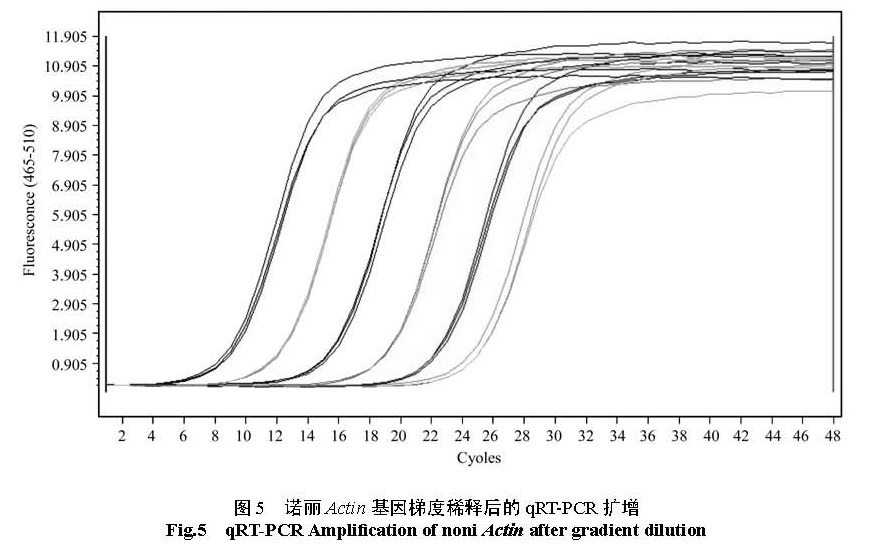
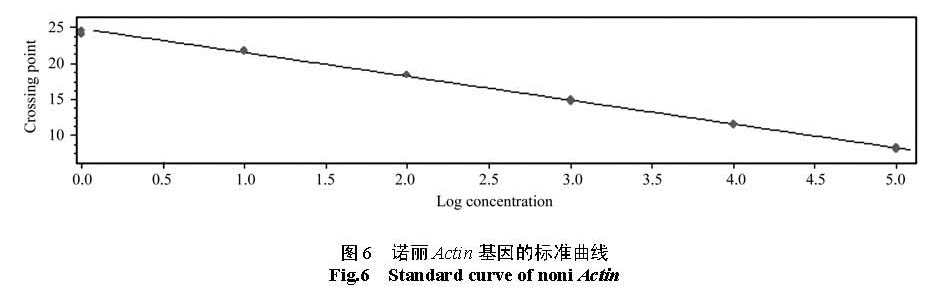
2.4 诺丽 Actin基因的 qRT-PCR体系以其中一份阳性 cDNA样品梯度稀释后进行 qRT-PCR 扩增,得到了扩增曲线(图5)和标准曲线(图6)。结果表明,以 Ct值作为纵坐标( Y),以稀释倍数的对数为横坐标( X)建立的相对定量
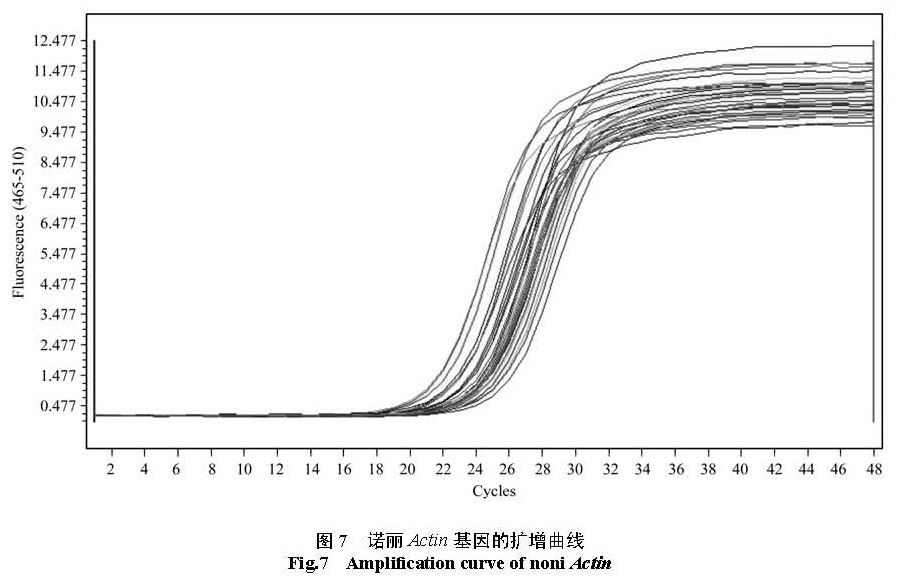
标准曲线,在所使用的浓度范围内具有良好的线性关系(R2=0.997 4),扩增效率为 101.4%。2.5 诺丽 Actin基因在诺丽不同器官及不同发育时期果实中的表达分析qRT-PCR的结果表明,诺丽 Actin基因在不同熟期的诺丽果实( 1-6号样品)中的 Ct值分布在
21.9~ 23.2,其中在完全成熟的诺丽果实中的 Ct值最大,基因表达丰度最低;诺丽 Actin基因在不同幼嫩程度的诺丽叶片( 7-9号样品)中的 Ct值分布在 23.7~ 24.5,Ct值相近,说明该基因在不同幼嫩程度的诺丽叶片中表达量基本一致;诺丽 Actin基因在全花和茎中的 Ct值分别为 21.2和 21.7,表达量基本一致。由此可知,诺丽 Actin基因在诺丽的各个组织、果实不同发育时期都有表达,因此推断诺丽 Actin基因为组成型表达的肌动蛋白基因,适宜将其作为研究诺丽其他基因表达的内参基因。
3 讨论
如果要进行基因表达量的研究,不论是半定量 RT-PCR还是 qRT-PCR,首先要找到相应的内参基因进行校正和标准化,主要是为了尽量避免不同样品在 RNA质量、反转录效率和 PCR反应条件上的差异 [20-21]。在 qRT-PCR分析中,可以有多种类型的看家基因作为内参基因,如甘油醛 -3-磷酸脱氢酶基因( Glyceral-Dehyde-3-Phosphate Dehydrogenase,GAPDH)、微管蛋白基因(α-Tubulin)、肌动蛋白基因( Actin)、转录延伸因子基因( Elongation Factors 1 alpha,EF-lα)、泛素基因( Ubiquitin)、18S rRNA基因等 [22-23]。但在大多植物的表达研究中, Actin基因家族是使用最频繁的看家基因,因为其在核苷酸和氨基酸水平均具有高度的保守性和同源性,且在各组织器官中表达恒定 [24-25]。鉴于此,本研究首先考虑用诺丽 Actin基因作为研究诺丽基因表达的内参基因。
本研究克隆了诺丽 Actin基因,填补了诺丽内参基因研究领域的空白,丰富了高等植物 Actin基因数据库,为进一步深入研究植物 Actin的功能、保守结构域、变异性及其起源进化等提供了新的数据。其他研究者再进行诺丽基因表达研究时,
可以直接使用 P3、P4作为荧光定量 PCR引物,也可以借鉴本研究测序得到的序列自行设计符合相应研究所需的 qRT-PCR引物。本研究还考察了诺丽 Actin基因的 qRT-PCR表达模式,通常理想的内参基因除了能在各组织细胞及各种处理下稳定表达外,其表达丰度还不应过高, qRT-PCR过程中,内参基因的 Ct值一般应在 15~ 30之间,太大或太小都会降低定量的准确性 [26],本研究在反转录 RNA量为 200 ng条件下,诺丽的 Ct值均在 21~ 24,表明表达丰度适宜, Actin基因适合做诺丽的内参基因。然而,随着植物内参基因的研究深入,越来越多的研究表明,在同一植物中同一内参基因的稳定性在不同生理条件下通常并不恒定,且在不同物种中同源的内参基因也没有绝对的通用性,因此,在所有条件下都稳定表达的理想内参基因并不存在 [27]。在 qRT-PCR分析中,同时使用两个或多个内参基因有助于调整系统偏差,更有利于得到准确的基因表达结果 [28]。因此,后续研究可以调取诺丽其他内参基因,如 GAPDH基因、 18S rRNA基因、α-tubulin基因、Ubipuitin基因等,同时利用 BestKeeper、geNorm和 NormFinder等内参基因分析软件,根据统计学方法进行筛选,为诺丽基因表达研究提供稳定的、可靠的和重复性高的最优内参基因。
- [1] 贺淹才 . 肌动蛋白和肌动蛋白基因的研究进展 [J]. 生命的化学 , 2002, 22(3): 248-250.
- [2] 陈颖 , 王刚 , 赵俊霞 . 高等植物体内的肌动蛋白 [J]. 生物学通报 , 2003, 38(2): 13-15.
- [3] 王洪振 , 程焉平 . 细胞核内肌动蛋白参与基因转录的研究进展 [J]. 吉林师范大学学报 (自然科学版 ), 2005, 2: 34-36.
- [4] Li J, Henty-Ridilla J L, Huang S, et al. Capping protein modulates the dynam is behavior of actin filamentsin response to phosphatidic acid in Arabidopsis [J]. Plant Cell, 2012, 24(9): 3742-3754.
- [5] Smertenko A, Franklin-Tong V E. Organisation and regulation of the cytoskeleton in plant programmed cell death [J]. Cell Death Differ., 2011, 18: 1263-1270.
- [6] 李远华 , 陆建良 , 范方媛 , 等 . 茶树根系 Actin基因克隆及表达分析 [J]. 茶叶科学 , 2015, 35(4): 336-346.
- [7] 李园莉 , 江元清 . 向日葵肌动蛋白基因的 cDNA克隆及进化分析 [J]. 农业生物技术学报 , 2002, 10(1): 67-71.
- [8] 杨丽霞 , 李玲 . 花生肌动蛋白基因的克隆及序列分析 [J]. 花生学报 , 2007, 35(4): 6-9.
- [9] 马清 , 周向睿 , 伍国强 , 等 . 盐生植物碱蓬 Actin基因片段的克隆及序列分析 [J]. 生物技术 , 2009, 19(1): 1-3.
- [10] 许娟 , 罗兴录 . 木薯 Actin基因片段的克隆及序列分析 [J]. 生物技术通报 , 2011(6): 65-70.
- [11] 范丙友 , 李芳 , 张文婷 , 等 . 芍药肌动蛋白基因的克隆及表达分析 [J]. 中草药 , 2013, 44(15): 2136-2142.
- [12] 蔡深文 , 熊治廷 , 刘晨 , 等 . 海州香薷 Actin基因片段克隆及表达分析 [J]. 生物技术通报 , 2015, 31(2): 111-115.
- [13] 龚明霞 , 周芸伊 , 王爱勤 , 等 . 山药 Actin基因片段的克隆及表达分析 [J]. 生物技术通报 , 2016, 32(7): 73-80.
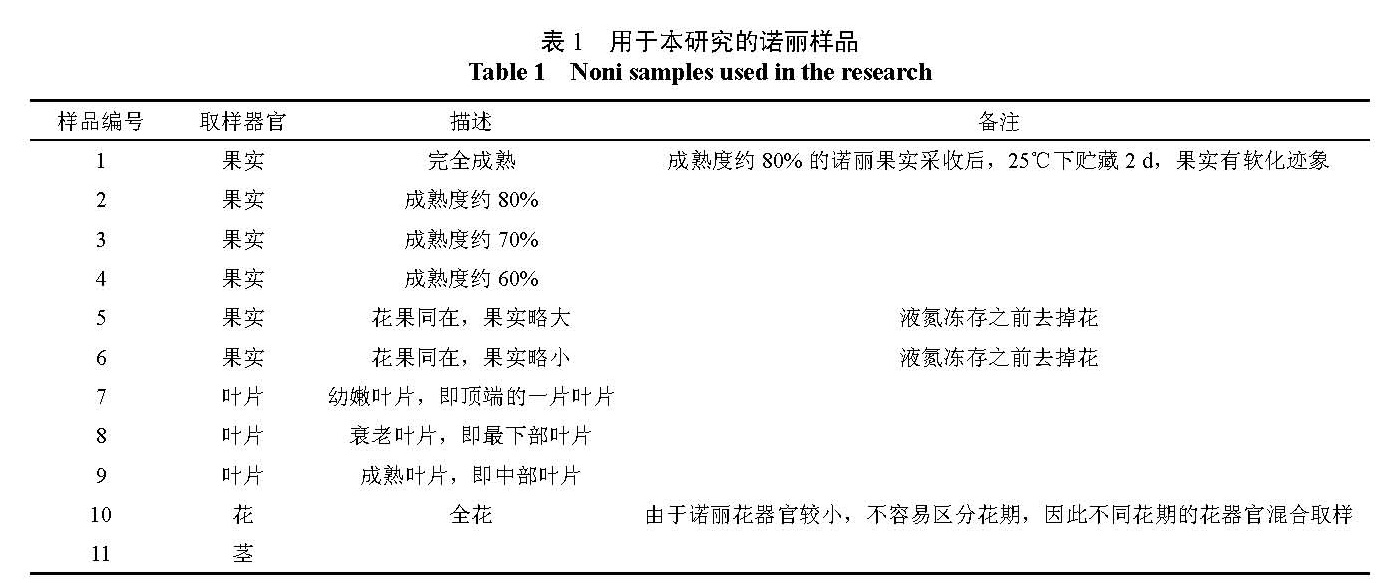
1.1 实验材料将成熟度约 80%的诺丽果实采收后, 25 ℃下贮藏 2 d后作为基因克隆的植物材料。用于 qRT-PCR的植物材料分别为诺丽不同熟期的果实、诺丽叶片、诺丽全花、诺丽茎段等(表1)。诺丽样品采自于云南省玉溪市元江县诺丽种植基地,于保鲜盒中带回实验室,除 1号样品外,其他样品用液氮速冻,暂存于 -70 ℃冰箱待用; 1号样品于 25 ℃下贮藏 2 d后用液氮速冻,暂存于 -70 ℃冰箱待用。大肠杆菌 DH5α菌株由本实验保存。
1.2 主要试剂柱式 Trizol总 RNA提取试剂盒(生工 B511321)、M-MuLV First Strand cDNA Synthesis Kit M-MuLV第一链 cDNA合成试剂盒(生工 B532435)、第一链 cDNA合成试剂盒( RevertAid Premium Reverse Transcriptase)、 LA Taq (TaKaRa DRR02AG)、2×GC Buffer I、Marker(BBI B600032)、柱式 DNA胶回收试剂盒(生工 B518131)、定量 PCR试剂 SG Fast qPCR Master Mix(Roche 罗氏)、溴化乙锭、琼脂糖等均购自于上海生工。
1.3 实验方法1.3.1 总 RNA的提取与反转录总 RNA的提取按照柱式 Trizol总 RNA提取试剂盒说明书进行。总 RNA提取后通过电泳检测其完整性,通过吸光值法检测其浓度。 cDNA第一链的合成按照试剂盒说明书进行。
1.3.2 引物的设计与合成通过对甜橙( LOC102622338)、玉兰(AF281323)、白桦(EU588981)、桑树(DQ785808)、白杨( EF418792)等几种植物 Actin基因的核苷酸序列进行同源性比较,找出高度保守的区段,根据同源性高和简并性低的原则,利用 Primer Premier 5.0软件设计一对简并引物 P1:5’-GGAACTGGAATGGTSAAGGCT-3’、 P2:5’-CCACATCTGYTGGAAGGTGCT-3’, 其中:S=G/C,Y=C/T,用于扩增诺丽 Actin基因片段,预测目的片段的长度为 400 bp。根据上述扩增的片段设计一对用于 qRT-PCR的引物,上游引物 P3: 5’-TGTATGGCAACATCGTTCTCAGT-3’,下游引物 P4:5’-CCACCTTAATCTTCATGCTGCT-3’,预计扩增长度 111 bp。引物由上海生工合成。
1.3.3 诺丽 Actin基因片段的扩增PCR反应体系为 25 µL,包括 ddH2O 6.3 µL, 2×GC Buffer I 12.5 µL,简并引物 P1(10 µmol)、 P2(10 µmol)各 0.5 µL,dNTPs(2.5 mM)4 µL, cDNA 1 µL,LA Taq酶(5 U/µL)0.2 µL。PCR反应条件为: 95 ℃预变性 3 min,94 ℃变性 30 s, 55 ℃退火 30 s,72 ℃延伸 60 s,33个循环后 72 ℃充分延伸 7 min。PCR 扩增产物用 1.5%琼脂糖凝胶、 1×TAE电泳缓冲液进行检测,紫外透射光下观察并拍照。目的片段的回收和纯化按照试剂盒操作说明进行。
1.3.4 阳性克隆的筛选与鉴定回收的 PCR 产物连接到 pMD-18T载体,热激法转化大肠杆菌 DH5α感受态细胞,用 LB固体培养基(含有 50 μg/mL氨苄青霉素)进行筛选,阳性克隆经菌落 PCR 鉴定确认后,送至上海生工测序。
1.3.5 序列的生物信息学分析序列的比较、翻译等在 DNAMAN 生物软件上进行,Blastx在 NCBI网站上进行。
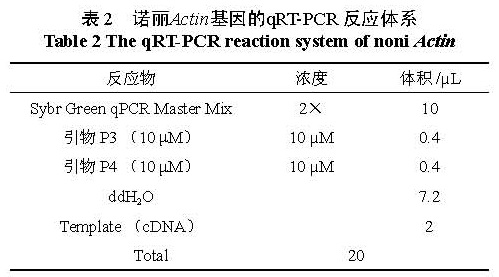
1.3.6 诺丽 Actin基因的 qRT-PCR1.3.6.1 反应体系采用 SYBR Green染料法,在 Light Cycler 480 Software Setup(Roche 罗氏)荧光定量 PCR 仪上进行扩增和数据分析。在本课题组进行前期 qRT-PCR过程中确定的最佳扩增体系(表2)和反应条件进行实验,扩增条件为: 95 ℃ 3 min充分变性后进入下述 48个循环,95 ℃ 7 s,57 ℃ 10 s,75 ℃ 10 s。
1.3.6.2 熔解曲线分析和标准曲线的建立首先进行普通 PCR反应,得到的 PCR产物用 1%琼脂糖凝胶电泳检测,以确定得到的产物是否为目的产物,再对 qRT-PCR产物熔解峰进行分析。以其中一份阳性样品 cDNA进行 1倍、10倍、100倍、1 000倍、10 000倍、100 000倍的梯度稀释作为模板,采用优化好的 PCR反应条件进行 qRT-PCR,取 6个点制作标准曲线。由方程 E=(10-1/ slope-1)×100%计算出引物的扩增效率,扩增效率在 95%至 110%即符合要求。
1.3.6.3 诺丽不同器官及不同发育时期果实的 qRTPCR分析将诺丽不同组织提取的 RNA分别取 200 ng进行反转录,然后进行 qRT-PCR分析。

学报简介
中南林业科技大学学报
《中南林业科技大学学报》原名《中南林学院学报》,是中南林业科技大学主办的以林为特色的自然科学学术期刊。该刊1981年创刊,2010变更为月刊,月底出版,国内外公开发行。国际刊号为ISSN 1673-923X,国内刊号为CN43-1470/S。该刊是教育部优秀科技期刊,全国优秀高校学报,湖南省一级期刊。是全国中文核心期刊,中国科学引文数据库来源期刊,中国精品科技期刊,中国科技核心期刊。该刊入编了国内所有的期刊数据库。
主要栏目:林学、生态学、生物科学与技术、植物学、园林、木材科学等。
读者对象:本刊适合于农林院校师生以及农林科研院所、农林管理部门和生产单位的科技和管理人员阅读,也适合于与以上学科和专业有关的其他高校师生和科技人员阅读。